In uno studio rivoluzionario pubblicato di recente su Cell Host & Microbe, i ricercatori della Georgia State University Institute for Biomedical Sciences hanno svelato un’importante connessione tra la composizione del microbiota intestinale e la gravità delle infezioni virali respiratorie (IVR). Il lavoro, intitolato “Intestinal Microbiota Programming of Alveolar Macrophages Influences Severity of Respiratory Viral Infection,” fornisce approfondimenti convincenti sul ruolo dei batteri filamentosi segmentati (Segmented Filamentous Bacteria, SFB) nel fortificare i topi contro una serie di virus respiratori, tra cui influenza, virus respiratorio sinciziale (RSV) e il coronavirus della sindrome respiratoria acuta grave 2 (SARS-CoV-2).
Interazione tra microbiota intestinale e risposta immunitaria ai virus respiratori
Lo studio, gestito da Andrew Gewirtz, Regents’ Professor presso l’Institute for Biomedical Sciences della Georgia State, e Richard Plemper, Regents’ Professor e direttore del Center for Translational Antiviral Research, getta luce sull’interazione intricata tra il microbiota intestinale e la risposta immunitaria ai virus respiratori.
La loro ricerca si è concentrata su topi con variazioni distinte del microbioma, indagando sull’impatto del microbiota intestinale sulla suscettibilità e gravità delle infezioni da virus respiratori. In particolare, è stato osservato che la presenza o l’assenza degli SFB giocava un ruolo importante nella definizione degli esiti delle infezioni virali. Sia che fossero acquisiti naturalmente o somministrate, gli SFB mostravano un notevole effetto protettivo contro il virus dell’influenza. Lo stesso effetto è stato rilevato anche contro RSV e SARS-CoV-2.
Gli autori hanno sottolineato l’importanza della composizione del microbiota intestinale, affermando: “Abbiamo ipotizzato che un fattore importante sia la composizione del microbiota intestinale, che ora è riconosciuta per avere un’ampia influenza su una serie di malattie infiammatorie croniche e sulle risposte immunitarie associate a tali malattie.”
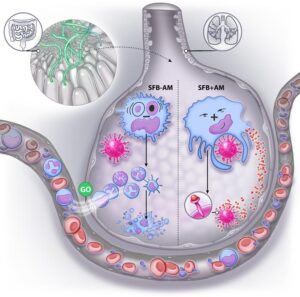
Modulazione dei macrofagi alveolari
Una delle scoperte cruciali dello studio risiede nella modulazione dei macrofagi alveolari, le cellule immunitarie situate nei polmoni che agiscono come primi soccorritori alle minacce inalate, inclusi i virus respiratori. Nei topi privi di SFB, si è verificato un rapido svuotamento di questi macrofagi alveolari durante la progressione dell’infezione da virus dell’influenza A. Tuttavia, nei topi colonizzati da SFB, queste cellule immunitarie sono state in qualche modo alterate per acquisire resistenza alla deplezione indotta dal virus dell’influenza e alla segnalazione infiammatoria.
Come notano i ricercatori: “Mostriamo quindi che il modo in cui i macrofagi alveolari rispondono ai virus respiratori è drasticamente alterato dalla composizione del microbiota intestinale. In particolare, abbiamo riportato che la colonizzazione dell’intestino da parte di SFB, acquisita naturalmente o somministrata dall’esterno, attenua marcatamente l’espressione genica pro-infiammatoria dei macrofagi alveolari indotta dai virus dell’influenza A, aumentando contemporaneamente la capacità dei macrofagi alveolari di disabilitare il virus.”
Importanza del Sistema del Complemento
Inoltre, lo studio ha evidenziato il ruolo cruciale del sistema del complemento, un’importante componente del sistema immunitario, nella difesa contro il virus dell’influenza. In effetti, i macrofagi alveolari, stimolati dagli SFB, hanno disabilitato il virus tramite l’attivazione del sistema del complemento, fornendo così uno strato di protezione contro le gravi infezioni respiratorie.
I risultati collettivi indicano che affinché gli SFB esercitino la loro influenza protettiva, è essenziale la presenza di macrofagi alveolari nei polmoni. Questa rivelazione ha implicazioni significative per comprendere le dinamiche delle infezioni respiratorie negli esseri umani, offrendo potenzialmente una nuova strada per la valutazione del rischio riguardo alla progressione verso malattie gravi a seguito dell’infezione.
Prospettive future
Nel concludere il loro studio, gli autori offrono una prospettiva orientata al futuro, affermando: “È altamente improbabile che le SFB siano l’unico microbiota intestinale in grado di influenzare i macrofagi alveolari e la suscettibilità alle IVR. Piuttosto, ipotizziamo che i macrofagi alveolari siano un componente chiave dell’asse intestino-polmone, in cui il microbiota di un individuo nella sua interezza è un determinante dell’esito della malattia dopo l’esposizione a una serie di virus respiratori.”
Mentre la comunità scientifica continua a svelare le complessità dell’asse intestino-polmone, queste scoperte aprono la strada ad approcci innovativi nella manipolazione del microbiota intestinale per potenziare le difese immunitarie contro le infezioni virali respiratorie, rivoluzionando potenzialmente le strategie al fine di prevenire e trattare tali malattie in futuro.