In un’epoca in cui la resistenza agli antibiotici minaccia di minare la medicina moderna, i ricercatori hanno fatto una scoperta rivoluzionaria che potrebbe rivitalizzare la nostra capacità di trattare le infezioni batteriche mortali. Un recente studio di Wang et al. rivela come minuscoli messaggeri cellulari possono silenziare i geni che rendono i batteri resistenti agli antibiotici, fornendo così una potenziale nuova arma nella lotta contro i superbatteri.
Il problema: La crescita dei superbatteri
L’emergere di batteri multi-resistenti ai farmaci è diventata una delle sfide sanitarie globali più pressanti del nostro tempo. Questi ‘superbatteri’ hanno sviluppato meccanismi in grado di resistere anche agli antibiotici più potenti, riducendo così le opzioni di trattamento a disposizione dei medici per infezioni potenzialmente letali.
Un patogeno particolarmente preoccupante è lo Staphylococcus aureus resistente alla meticillina (MRSA), che ha sviluppato resistenza agli antibiotici beta-lattamici attraverso un gene chiamato mecA. Questo gene produce una proteina nota come proteina legante la penicillina 2a (PBP2a), la quale permette al batterio di sopravvivere al trattamento con meticillina. Lo sviluppo tradizionale di antibiotici non riesce a tenere il passo con la rapida evoluzione della resistenza batterica e questo crea un urgente bisogno di approcci terapeutici alternativi.
La svolta: silenziare i geni della resistenza
Il team di ricerca ha scoperto che minuscole strutture simili a bolle, chiamate esosomi — naturalmente rilasciate dalle cellule umane per scambiarsi materiali— possono essere caricate con piccoli RNA interferenti (siRNA) e consegnate alle cellule batteriche. Questi siRNA sono progettati per mirare e silenziare specifici geni batterici. Fino ad ora, i ricercatori non potevano ottenere l’interferenza dell’RNA (RNAi) nei batteri perché questi microrganismi mancano del macchinario cellulare necessario. Tuttavia, l’innovazione presentata in questo studio dimostra che gli esosomi umani possono trasportare non solo il siRNA, ma anche l’intero macchinario necessario, inclusa una proteina cruciale chiamata Argonaute 2 (AGO2), direttamente nelle cellule batteriche, permettendo così l’attivazione dell’RNAi anche all’interno di queste ultime.
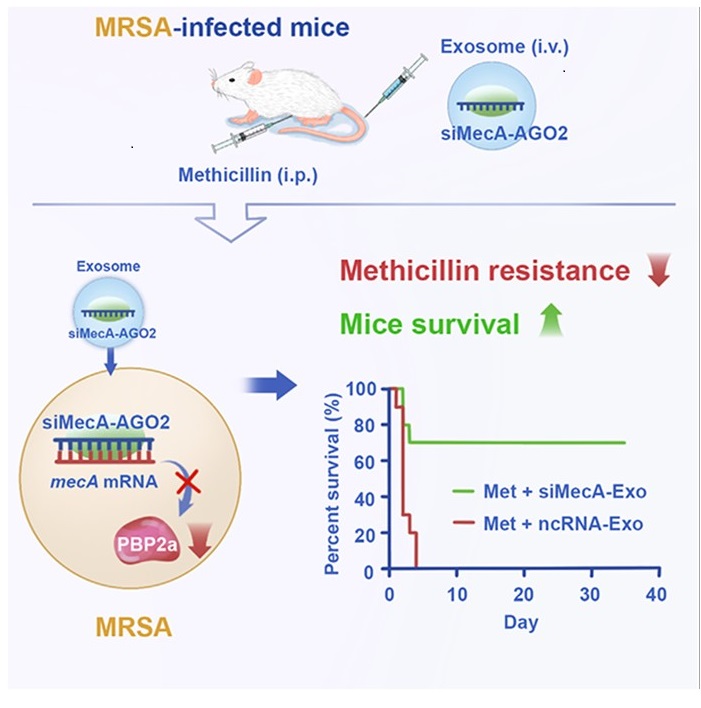
Come funziona la tecnologia
I ricercatori hanno seguito un approccio sistematico per sviluppare e validare la loro tecnologia.
Innanzitutto, hanno ingegnerizzato cellule umane per produrre esosomi contenenti siRNA, progettati per mirare a specifici geni di resistenza batterica. Questi esosomi trasportano efficacemente il loro carico nelle cellule batteriche, con ogni batterio che riceve approssimativamente 56-105 copie di siRNA. Successivamente, la proteina AGO2 esosomiale forma un complesso con siRNA, legandosi all’RNA messaggero batterico e prevenendo la sintesi proteica senza distruggere l’mRNA—un processo chiamato repressione traduzionale.
Infine, mirando specificamente al gene mecA nell’MRSA, i ricercatori sono stati in grado di ridurre l’espressione della proteina PBP2a e di ripristinare la suscettibilità del batterio alla meticillina. Durante questo processo, il team di ricerca ha fatto una scoperta importante: a differenza delle cellule umane, dove i siRNA perfettamente abbinati causano tipicamente la degradazione dell’mRNA, nei batteri, il complesso siRNA-AGO2 blocca principalmente la traduzione senza degradare l’mRNA bersaglio. Questo rappresenta un nuovo meccanismo di silenziamento genico.
Mettere il sistema alla prova: esperimenti di laboratorio
Il team di ricerca ha condotto una serie di test per verificare il loro approccio, trattando l’MRSA con con siMecA-Exos (esosomi contenenti siRNA mirati a mecA) in culture di laboratorio. l’MRSA così trattato ha mostrato livelli di proteina PBP2a significativamente diminuiti, una riduzione di due volte nella concentrazione minima inibitoria (MIC) della meticillina, e un numero aumentato di cellule batteriche uccise quando queste vengono trattati con la combinazione di siMecA-Exos e meticillina. Inoltre, i ricercatori hanno confermato che la proteina esosomiale AGO2 è essenziale per questo effetto di silenziamento genico: infatti, quando gli esosomi venivano preparati da cellule con livelli ridotti di AGO2, l’effetto terapeutico risultava in gran parte perduto.
Dal laboratorio agli organismi viventi: modelli murini
Andando oltre gli esperimenti di laboratorio, i ricercatori hanno testato il loro approccio negli animali viventi, in particolare in topi BALB/c.
I topi BALB/c, infettati con dosi letali di MRSA, hanno ricevuto trattamenti giornalieri di meticillina combinata con siMecA-Exos. I risultati sono stati notevoli: il 70% dei topi è sopravvissuto dopo essere stato trattato con la terapia combinata, rispetto a una mortalità quasi completa nei gruppi di controllo che ricevevano solo meticillina o meticillina con esosomi di controllo. Le cariche batteriche sono state significativamente ridotte nel sangue, nel fegato, nella milza e nei reni dei topi trattati. I marcatori infiammatori sono diminuiti, indicando una ridotta gravità dell’infezione. L’analisi degli MRSA isolati dai topi trattati ha confermato la presenza sia del siMecA sia della proteina AGO2 all’interno dei batteri, insieme a una ridotta espressione di PBP2a, confermando così che il meccanismo osservato negli esperimenti di laboratorio è attivo anche all’interno di un organismo vivente.
Innovazione nella consegna: esosomi auto-assemblati
Considerando anche le potenziali sfide associale alla produzione di esosomi per uso terapeutico, i ricercatori hanno sviluppato una soluzione ingegnosa sfruttando la naturale capacità di produzione del corpo. In particolare, gli studiosi hanno progettato un circuito genetico che, quando iniettato nei topi, programma le cellule epatiche degli animali alla produzione e al rilascio di esosomi contenenti il siRNA desiderato.
Questo approccio offre vantaggi significativi: elimina le complicate procedure di produzione e purificazione, evita potenziali preoccupazioni di immunogenicità e cancerogenicità associate a esosomi estranei, e raggiunge concentrazioni biologicamente efficaci di siRNA negli esosomi circolanti. I risultati sono stati convincenti: i topi infettati con dosi letali di MRSA e trattati con meticillina più il circuito genetico siMecA hanno mostrato un tasso di sopravvivenza del 90% su un periodo di osservazione di 35 giorni, delle cariche batteriche significativamente ridotte nel sangue e negli organi, e un’efficacia costante contro molteplici ceppi di MRSA.
Implicazioni per il futuro della terapia antibiotica
Questa rivoluzionaria ricerca apre diverse strade promettenti per affrontare la resistenza agli antibiotici. A differenza degli antibiotici tradizionali, i quali richiedono un’estesa rimodellazione chimica per superare le mutazioni di resistenza, l’approccio siRNA può essere rapidamente adattato semplicemente cambiando la sequenza di RNA per abbinarla a nuovi geni bersaglio. La scoperta solleva anche domande intriganti sul fatto che i mammiferi utilizzino naturalmente gli esosomi per regolare il loro microbioma attraverso la comunicazione tra specie. Piuttosto che sostituire gli antibiotici, questo approccio potrebbe rivitalizzare quelli esistenti silenziando i meccanismi di resistenza, estendendo in questo modo la vita utile del nostro attuale arsenale antibiotico.
Sfide da superare
Nonostante le sue promesse, diverse limitazioni devono essere affrontate prima che questa tecnologia possa raggiungere l’applicazione clinica. Il meccanismo preciso con cui il complesso siRNA-AGO2 inibisce la traduzione proteica batterica richiede ulteriori indagini. Gli attuali metodi di purificazione degli esosomi potrebbero necessitare di perfezionamenti per garantire la specificità. Inoltre, sono necessari studi su una gamma più ampia di ceppi e modelli batterici per generalizzare i risultati. In ultimo, la ricerca si è concentrata sulla meticillina, che oggi è raramente usata nella pratica clinica, mentre sarebbero necessari altri studi per testare l’approccio con gli antibiotici attualmente utilizzati.


Lascia un commento